科大團隊研發出新技術,透過提升合成信使核糖核酸(mRNA)生產蛋白質的效率,從而提升治療癌症或武肺疫苗的效用。有關發現已在科學期刊《分子療法 一核酸》的線上版發表。
mRNA是一種是複製自細胞核內的去氧核糖核酸(DNA)的遺傳物質,作用好像信使一樣,用來指示身體製造特定蛋白質。合成mRNA是近年用以製造疫苗和藥物的新興技術,能有效指導細胞生產不同的蛋白質來治療癌症和對抗病毒等。不過其跟傳統藥物一樣,要製造足夠的蛋白質,病人便需要注射較高劑量,同時亦要多次使用。
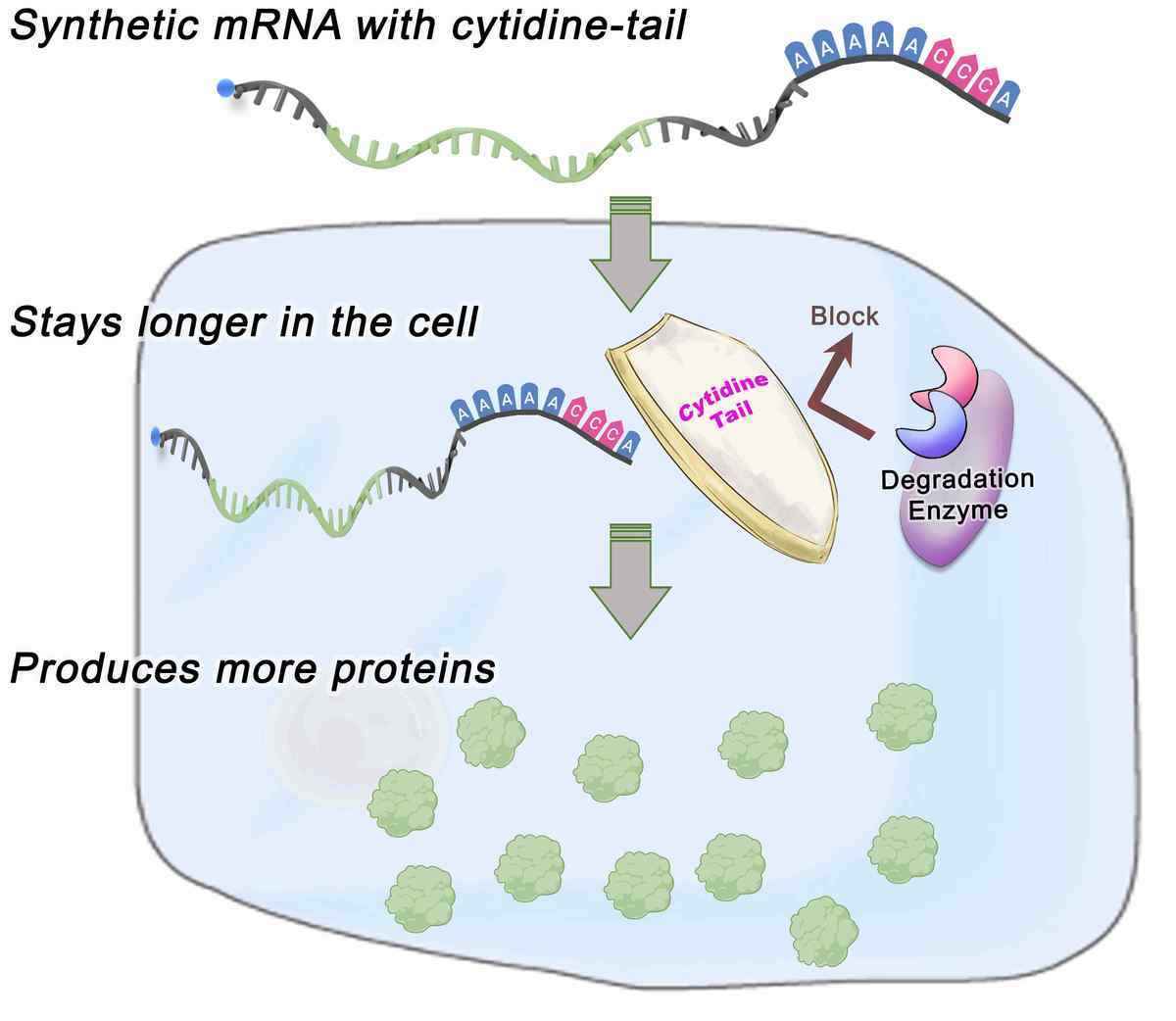
科大團隊花三年研究改進mRNA技術,反覆測試mRNA尾鏈序列的不同組合,領導團隊的化學及生物工程學系助理教授曠怡解釋,mRNA產出蛋白質再在體內產生抗原,抗原繼而再生成抗體,當蛋白質愈多,效率愈高。她提到,過去科學界專注在mRNA的「頭」及「中間」研究,但甚少研究mRNA尾鏈序列,慣用化學物質「嘌呤A」作尾鏈,團隊通過在尾鏈加入化學物質「嘧啶C」,減慢分解時間,從而產生更多的蛋白質。
研究顯示,新型尾鏈序列較一般合成mRNA的普通尾鏈序列相比,能在人類細胞及小鼠身上生產多3至10倍蛋白質,而生產蛋白質的持續時間亦延長了一倍,一般舊技術會在體內存在1日,而新型尾鏈序列的mRNA能在存在體內48小時後仍有產能,直至72小時後才完全消失,令到療效更顯著和持久。
曠怡表示,不同的mRNA都會受益於改進後的尾鏈序列,而且不增加成本,更可以與現有的技術並用,即使mRNA的容量減半,仍可生產更多蛋白質,相信日後能同時降低治療成本。
她又指,團隊現正與中山大學合作進行癌症疫苗的動物實驗,期待與藥廠合作,盡快將新技術投入臨床實驗,希望最少能讓藥物效用提高三倍,同時不額外增加成本,「打少啲針,病人都冇咁痛苦(少打數針,病人都沒這麼痛苦)」。@
------------------
【堅守真相與傳統】21周年贊助活動🎉:
https://www.epochtimeshk.org/21st-anniv
🔥專題:全球通脹加息📊
https://bit.ly/EpochTimesHK_GlobalInflation
🗞紀紙:
https://bit.ly/EpochTimesHK_EpochPaper
✒️名家專欄:
https://bit.ly/EpochTimesHK_Column
-------------------
局勢持續演變
與您見證世界格局重塑
-------------------
🔔下載大紀元App 接收即時新聞通知:
🍎iOS:https://bit.ly/epochhkios
🤖Android:https://bit.ly/epochhkand
📰周末版實體報銷售點👇🏻
http://epochtimeshk.org/stores